„CRISPR-Cas системите“ в бактериите и вирусите идентифицират и унищожават нахлуващите вирусни последователности. Това е бактериална и археална имунна система за защита срещу вирусни инфекции. През 2012 г. системата CRISPR-Cas беше призната за a геном инструмент за редактиране. Оттогава широка гама от системи CRISPR-Cas са разработени и са намерили приложения в области като генна терапия, диагностика, изследвания и подобряване на културите. Въпреки това наличните в момента системи CRISPR-Cas имат ограничена клинична употреба поради честите случаи на редактиране извън целта, неочаквани ДНК мутации и наследствени проблеми. Изследователите наскоро съобщиха за нова система CRISPR-Cas, която може да насочва и унищожава иРНК и протеини свързани с различни генетични заболявания по-точно без нецелеви въздействия и наследствени проблеми. Наречен Craspase, това е първата CRISPR-Cas система, която показва протеин функция за редактиране. Това е и първата система, която може да редактира както РНК, така и протеин. Тъй като Craspase преодолява много ограничения на съществуващите системи CRISPR-Cas, той има потенциал да революционизира генната терапия, диагностиката и мониторинга, биомедицинските изследвания и подобряването на културите.
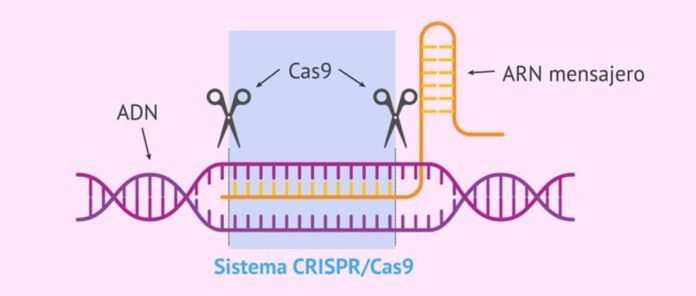
„CRISPR-Cas система“ е естествена имунна система от бактерии и археи срещу вирусни инфекции, която идентифицира, свързва и разгражда последователностите във вирусния ген, за да защити. Състои се от две части – бактериална РНК, транскрибирана от вирусния ген, включен в бактериалния геном след първата инфекция (наречен CRISPR, това идентифицира целевите последователности на нахлуващите вирусни гени) и свързан разрушител протеин наречен „Свързан с CRISPR протеин (Cas)”, който свързва и разгражда идентифицираните последователности във вирусния ген, за да предпази бактериите от вируси.
ЯСНО означава „групирани редовно разположени кратки палиндромни повторения“. Това е транскрибирана бактериална РНК, характеризираща се с палиндромни повторения.
Палиндромните повторения (CRISPRs) са открити за първи път в последователностите на E. коли през 1987 г. През 1995 г. Франсиско Мохика наблюдава подобни структури в археи и той е първият, който ги смята за част от имунната система на бактериите и археите. През 2008 г. за първи път беше експериментално демонстрирано, че целта на имунната система на бактериите и археите е чужда ДНК, а не иРНК. Механизмът за идентифициране и разграждане на вирусни последователности предполага, че такива системи могат да се използват като инструмент за редактиране на генома. От признаването си като инструмент за редактиране на геном през 2012 г. системата CRISPR-Cas измина много дълъг път като твърдо установен стандарт ген редактиране система и е намерил широк спектър от приложения в биомедицината, селското стопанство, фармацевтичните индустрии, включително в клиничната генна терапия1,2.
Широка гама от CRISPR-Cas системите вече са идентифицирани и в момента са налични за наблюдение и редактиране на ДНК/РНК последователности за изследвания, скрининг на лекарства, диагностика и лечение. Настоящите системи CRISPR/Cas са разделени на 2 класа (клас 1 и 2) и шест типа (тип I до XI). Системите от клас 1 имат множество Cas протеини които трябва да образуват функционален комплекс, за да се свържат и да действат върху своите цели. От друга страна, системите от клас 2 имат само един голям Cas протеин за свързване и разграждане на целеви последователности, което прави системите от клас 2 по-лесни за използване. Често използвани системи от клас 2 са Cas 9 тип II, Cas13 тип VI и Cas12 тип V. Тези системи може да имат нежелани съпътстващи ефекти, т.е. въздействие извън целта и цитотоксичност3,5.
Генни терапии въз основа на настоящите CRISPR-Cas системи имат ограничена клинична употреба поради честите случаи на редактиране извън целта, неочаквани ДНК мутации, включително големи заличавания на ДНК фрагменти и големи структурни варианти на ДНК както в прицелните, така и в нецелевите места, което води до клетъчна смърт и други наследствени проблеми.
Краспаза (или каспаза, ръководена от CRISPR)
Изследователите наскоро съобщиха за нова система CRISPER-Cas, която е система от клас 2 тип III-E Cas7-11, свързана с подобна на каспаза протеин следователно наречен Краспаза или CRISPR-насочвана каспаза 5 (Каспазите са цистеинови протеази, които играят ключова роля в апоптозата при разграждането на клетъчните структури). Има потенциални приложения в области като генна терапия и диагностика. Краспазата е РНК-насочвана и РНК-насочена и не се включва в ДНК последователностите. Може да насочва и унищожава иРНК и протеини свързани с различни генетични заболявания по-точно без нецелево въздействие. По този начин елиминирането на гени, свързани със заболявания, е възможно чрез разцепване на ниво иРНК или протеин. Освен това, когато се свърже със специфичен ензим, краспазата може да се използва и за модифициране на функциите на протеините. Когато функциите му на РНКаза и протеаза се премахнат, Краспаза се дезактивира (dКраспаза). Той няма режеща функция, но се свързва с РНК и протеинови последователности. Следователно dCraspase може да се използва в диагностиката и образната диагностика за наблюдение и диагностика на заболявания или вируси.
Craspase е първата CRISPR-Cas система, която показва функция за редактиране на протеини. Това е и първата система, която може да редактира както РНК, така и протеин. Това е ген редактиране функция идва с минимални нецелеви ефекти и без наследствени проблеми. Следователно Craspase вероятно ще бъде по-безопасен при клинична употреба и терапия в сравнение с други налични в момента системи CRISPR-Cas 4,5.
Тъй като Craspase преодолява много ограничения на съществуващите системи CRISPR-Cas, той има потенциал да революционизира генната терапия, диагностиката и мониторинга, биомедицинските изследвания и подобряването на културите. Необходими са повече изследвания, за да се разработи надеждна система за доставяне, за да се насочат точно гените, причиняващи заболявания в клетките, преди да се докаже безопасността и ефикасността в клинични изпитвания.
***
Литература:
- Gostimskaya, I. CRISPR–Cas9: История на откриването му и етични съображения за използването му при редактиране на генома. Биохимия Москва 87, 777–788 (2022). https://doi.org/10.1134/S0006297922080090
- Чао Ли и др 2022. Изчислителни инструменти и ресурси за редактиране на геном CRISPR/Cas. Геномика, протеомика и биоинформатика. Налично онлайн на 24 март 2022 г. DOI: https://doi.org/10.1016/j.gpb.2022.02.006
- van Beljouw, SPB, Sanders, J., Rodríguez-Molina, A. et al. РНК-насочени CRISPR-Cas системи. Nat Rev Microbiol 21, 21–34 (2023). https://doi.org/10.1038/s41579-022-00793-y
- Чуни Ху и др 2022. Craspase е CRISPR РНК-насочвана, РНК-активирана протеаза. Наука. 25 август 2022 г. Том 377, брой 6612. стр. 1278-1285. DOI: https://doi.org/10.1126/science.add5064
- Huo, G., Shepherd, J. & Pan, X. Craspase: Нов CRISPR/Cas редактор на двоен ген. Функционална и интегративна геномика 23, 98 (2023). Публикувано: 23 март 2023 г. DOI: https://doi.org/10.1007/s10142-023-01024-0
***